水质总大肠菌群、粪大肠菌群和大肠埃希氏菌的测定酶底物法

1、适用范围
本标准规定了测定水中总大肠菌群、粪大肠菌群和大肠埃希氏菌的酶底物法。
本标准适用于地表水、地下水、生活污水和工业废水中总大肠菌群、粪大肠菌群和大肠埃希氏菌的测定。本方法的检出限为10MPN/L。
2、规范性引用文件
本标准引用了下列文件或其中的条款。凡是不注日期的引用文件,其有效版本适用于本标准。
GB/T6682分析实验用水规格和实验方法
GB/T14581水质湖泊和水库采样技术指导
HJ494水质采样技术指导
HJ/T91地表水和污水监测技术规范
3、术语和定义
下列术语和定义适用于本标准。
3.1
总大肠菌群totalcoliforms
37℃培养24h,能产生β-半乳糖苷酶(β-D-galactosidase),分解选择性培养基中的邻硝基苯-β-D-吡喃半乳糖苷(ONPG)生成黄色的邻硝基苯酚的肠杆菌科细菌。
3.2
粪大肠菌群fecalcoliforms又称耐热大肠菌群(thermotolerantcoliforms)。44.5℃培养24h,能产生β-半乳糖苷酶(β-D-galactosidase),分解选择性培养基中的邻硝基苯-β-D-吡喃半乳糖苷(ONPG)生成黄色的邻硝基苯酚的肠杆菌科细菌。
3.3
大肠埃希氏菌Escherichiacoli俗称大肠杆菌。37℃培养24h,能产生β-半乳糖苷酶(β-D-galactosidase),分解选择性培养基中的邻硝基苯-β-D-吡喃半乳糖苷(ONPG)生成黄色的邻硝基苯酚,同时产生β-葡萄糖醛酸酶(β-Glucuronidase),分解选择性培养基中的4-甲基伞形酮-β-D-葡萄糖醛酸苷(MUG)释放出荧光物质(4-甲基伞形酮)的肠杆菌科细菌。
3.4
*大可能数mostprobablenumber(MPN)又称稀释培养计数,是一种基于泊松分布的间接计数法。利用统计学原理,根据一定体积不同稀释度样品经培养后产生的目标微生物阳性数,查表估算一定体积样品中目标微生物存在的数量(单位体积存在目标微生物的*大可能数)。
4、方法原理
在特定温度下培养特定的时间,总大肠菌群、粪大肠菌群、大肠埃希氏菌能产生β-半乳糖苷酶,将选择性培养基中的无色底物邻硝基苯-β-D-吡喃半乳糖苷(ONPG)分解为黄色的邻硝基苯酚(ONP);大肠埃希氏菌同时又能产生β-葡萄糖醛酸酶,将选择性培养基中的4-甲基伞形酮-β-D-葡萄糖醛酸苷(MUG)分解为4-甲基伞形酮,在紫外灯照射下产生荧光。统计阳性反应出现数量,查MPN表,分别计算样品中总大肠菌群、粪大肠菌群、大肠埃希氏菌的浓度值。
5、干扰和消除
5.1活性氯具有氧化性,能破坏微生物细胞内的酶活性,导致细胞死亡,可在样品采集(8.1)时加入硫代硫酸钠溶液(6.4)消除干扰。
5.2重金属离子具有细胞毒性,能破坏微生物细胞内的酶活性,导致细胞死亡,可在样品采集(8.1)时加入乙二胺四乙酸二钠溶液(6.5)消除干扰。
6、试剂和材料
除非另有说明,分析时均使用符合国家标准的分析纯试剂,实验用水应满足GB/T6682中三级水的要求。
6.1培养基。
本标准采用MinimalMediumONPG-MUG培养基。每100ml样品需使用培养基粉末。
2.7g±0.5g,所含基本成分如下:
硫酸铵[(NH4)2SO4]0.5g
硫酸锰(MnSO4)0.05mg
硫酸锌(ZnSO4)0.05mg
硫酸镁(MgSO4)10mg
氯化钠(NaCl)1g
氯化钙(CaCl2)5mg
亚硫酸钠(Na2SO3)4mg
两性霉素B(AmphotericinB)0.1mg
邻硝基苯-β-D-吡喃半乳糖苷(ONPG)50mg
4-甲基伞形酮-β-D-葡萄糖醛酸苷(MUG)7.5mg
茄属植物萃取物(Solanium萃取物)50mg
N-2-羟乙基哌嗪-N-2-乙磺酸钠盐(HEPES钠盐)0.53g
N-2-羟乙基哌嗪-N-2-乙磺酸(HEPES)0.69g
也可采用市售商品化培养基制品。
6.2硫代硫酸钠(Na2S2O3·5H2O)。
6.3乙二胺四乙酸二钠(C10H14N2O8Na2·2H2O)。
6.4硫代硫酸钠溶液:ρ(Na2S2O3)=0.10g/ml。称取15.7g硫代硫酸钠(6.2),溶于适量水中,定容至100ml,临用现配。
6.5乙二胺四乙酸二钠溶液:ρ(C10H14N2O8Na2·2H2O)=0.15g/ml。称取15g乙二胺四乙酸二钠(6.3),溶于适量水中,定容至100ml,此溶液保质期为30d。
6.697孔定量盘:含49个大孔,48个小孔。其中,每个小孔可容纳0.186ml样品,大孔中48个大孔每个可容纳1.86ml样品,一个顶部大孔可容纳11ml样品。也可采用经环氧乙烷灭菌的市售商品化成品。
6.7标准阳性比色盘。
6.8无菌水:取适量实验用水,经121℃高压蒸汽灭菌20min,备用。
7、仪器和设备
7.1采样瓶:具螺旋帽或磨口塞的100ml、250ml、500ml广口玻璃瓶。
注:在采集不存在或不考虑余氧、金属离子干扰的样品时,可采用市售无菌采样瓶或无菌采样袋。
7.2高压蒸汽灭菌器:121℃可调。
7.3恒温培养箱:允许温度偏差37℃±1℃、44.5℃±0.5℃。
7.4程控定量封口机:用于97孔定量盘(6.6)的封口。
7.5紫外灯:365~366nm。
7.6移液管:1ml±0.01ml、10ml±0.1ml。也可采用计量合格的可调式移液器。
7.7三角瓶:100ml。
7.8量筒:100ml±1ml。
7.9一般实验室常用仪器和设备。
注:三角瓶、移液管、采样瓶等玻璃器皿及采样器具要在试验前按无菌操作要求包扎,121℃高压蒸
汽灭菌20min,烘干,备用。
8、样品
8.1样品采集
点位布设及采样频次按照GB/T14581、HJ/T494和HJ/T91的相关规定执行。采集微生物样品时,采样瓶(7.1)不得用样品洗涤,采集样品于灭菌的采样瓶中。采集河流、湖库等地表水样品时,可握住瓶子下部直接将带塞采样瓶插入水中,约距水面10~15cm处,瓶口朝水流方向,拔瓶塞,使样品灌入瓶内然后盖上瓶塞,将采样瓶从水中取出。如果没有水流,可握住瓶子水平往前推。采样量一般为采样瓶容量的80%左右。样品采集完毕后,迅速扎上无菌包装纸。从龙头装置采集样品时,不要选用漏水龙头,采水前将龙头打开至*大,放水3~5min,然后将龙头关闭,用火焰灼烧约3min灭菌或用70%~75%的酒精对龙头进行消毒,开足龙头,再放水1min,以充分除去水管中的滞留杂质。采样时控制水流速度,小心接入瓶内。采集地表水、废水样品及一定深度的样品时,也可使用灭菌过的专用采样装置采样。在同一采样点进行分层采样时,应自上而下进行,以免不同层次的搅扰。如果采集的是含有活性氯的样品,需在采样瓶灭菌前加入硫代硫酸钠溶液(6.4),以除去活性氯对细菌的抑制作用(每125ml容积加入0.1ml的硫代硫酸钠溶液);如果采集的是重金属离子含量较高的样品,则在采样瓶灭菌前加入乙二胺四乙酸二钠溶液(6.5),以消除干扰(每125ml容积加入0.3ml的乙二胺四乙酸二钠溶液)。
注:15.7mg硫代硫酸钠(6.2)可去除样品中1.5mg活性氯,硫代硫酸钠用量可根据样品实际活性氯
量调整。
8.2样品保存
采样后应在2h内检测,否则,应10℃以下冷藏但不得超过6h。实验室接样后,不能立即开展检测的,将样品于4℃以下冷藏并在2h内检测。
9、分析步骤
9.1样品稀释
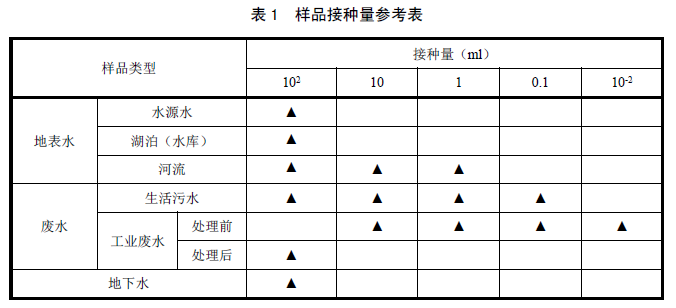
根据样品污染程度确定接种量(见表1),避免接种样品培养后97孔定量盘(6.6)出现全部阳性或全部阴性。接种量小于100ml时,应稀释样品后接种,接种量为10ml时,取10ml样品加入到盛有90ml无菌水(6.8)的三角瓶(7.7)中混匀制成1:10的稀释样品,其他接种量的稀释样品依次类推。对于未知样品,可选用多个接种量进行检测。
9.2接种
量取100ml样品或稀释样品于灭菌后的三角瓶,加入2.7g±0.5g培养基(6.1)粉末,充分混匀,完全溶解后,全部倒入97孔定量盘(6.6)内,以手抚平97孔定量盘背面,赶除孔内气泡,然后用程控定量封口机(7.4封口。观察97孔定量盘颜色,若出现类似或深于标准阳性比色盘(6.7)的颜色,则需排查样品、培养基、无菌水等一系列因素后,终止试验或重新操作
注:9.1、9.2步骤在野外操作时应避开明显局部污染源,建议使用一次性手套、口罩、酒精灯等。
9.3培养
测定总大肠菌群和大肠埃希氏菌时,将封口后的97孔定量盘放入恒温培养箱(7.3)中37℃±1℃下培养24h。测定粪大肠菌群时,将封口后的97孔定量盘放入的恒温培养箱中44.5℃±0.5℃下培养24h。
9.4对照试验
9.4.1空白对照
每次试验都要用无菌水(6.8)按照步骤9.1~9.3进行实验室空白测定。培养后的97孔定量盘不得有任何颜色反应,否则,该次样品测定结果无效,应查明原因后重新测定。
9.4.2阴性和阳性对照
总大肠菌群、大肠埃希氏菌、粪大肠菌群的阴性、阳性菌株参考表2。
|
检测指标
|
阳性菌种
|
阴性菌种
|
|
总大肠菌群
|
大肠埃希氏菌、
产气肠杆菌(Enterobacter aerogenes)
|
金黄色葡萄球菌(Staphylococcus aureus)、
假单胞菌属(Pseudomonas sp.)
|
大肠埃希氏
菌
|
大肠埃希氏菌
|
金黄色葡萄球菌、
假单胞菌属
|
|
粪大肠菌群
|
大肠埃希氏菌(耐热型)、
克雷伯氏菌属(Klebsiella trevisan)
(耐热型)
|
产气肠杆菌、
粪链球菌(Streptococcus faecalis)、
假单胞菌属
|
将标准菌株制成300~3000个/ml的菌悬液,将菌悬液按接种(9.2)和培养(9.3)要求操作,阳性菌株应呈现阳性反应;阴性菌株呈现阴性反应,否则,该次样品测定结果无效,应重新测定。
注:可先制备较高浓度菌悬液,采用血球计数器在显微镜下对其浓度进行初步测定,然后根据实际情
况用无菌水(6.8)稀释至300~3000个/ml。
9.4.3结果判读与计数
将培养24h后的97孔定量盘进行结果判读,样品变黄色判断为总大肠菌群或粪大肠菌群阳性;样品变黄色且在紫外灯(7.5)照射下有蓝色荧光,判断为大肠埃希氏菌阳性。如果结果可疑,可延长培养至28h进行结果判读,超过28h后出现的颜色反应不作为阳性结果。可使用保质期内的标准阳性比色盘以辅助判读,参见附录A。分别记录97孔定量盘中大孔和小孔的阳性孔数量。

